Percer les secrets de la maladie d'Alzheimer à l'échelle nanométrique
La maladie d'Alzheimer est une affection neurodégénérative débilitante qui touche des millions de personnes dans le monde. Elle est la principale cause de déclin cognitif et de décès chez les personnes âgées et représente environ 70% de toutes les maladies neurodégénératives. L'une des caractéristiques de la MA est l'accumulation de protéines amyloïdes-β (Aβ), qui forment des agrégats toxiques connus sous le nom de plaques amyloïdes. Pour mieux comprendre les mécanismes moléculaires de la maladie d'Alzheimer et mettre au point des traitements efficaces, les chercheurs explorent en permanence de nouvelles techniques pour étudier ces protéines à l'échelle nanométrique.
A étude de rupture dirigée par une équipe internationale de chercheurs, a démontré une nouvelle technique pour détecter les structures de feuillets Aβ dans les neurones individuels sans avoir recours à l'immunomarquage. Cette approche innovante, appelée microscopie optique à champ proche à balayage de type diffusion (s-SNOM), permet aux scientifiques d'analyser les structures à l'échelle nanométrique et de mieux comprendre la neurotoxicité causée par ces agrégats.
Comprendre les protéines amyloïdes-β
Les protéines Aβ sont associées à la maladie d'Alzheimer et leur accumulation dans le cerveau forme des plaques amyloïdes, toxiques pour les neurones. Les chercheurs pensent qu'en éliminant ces agrégats de protéines, ils peuvent ralentir la progression de la maladie. Cependant, les médicaments actuels ciblant les protéines Aβ n'ont pas été efficaces, ce qui indique que les mécanismes moléculaires de la neurotoxicité des protéines Aβ ne sont pas entièrement compris.
Les méthodes traditionnelles d'étude de ces protéines présentent des limites, telles qu'une résolution spatiale insuffisante ou la nécessité de connaître au préalable la structure de l'épitope ciblé pour le marquage du fluorophore. Pour surmonter ces difficultés, les chercheurs ont mis au point de nouvelles technologies de pointe telles que la s-SNOM, qui offre une imagerie à haute résolution à l'échelle nanométrique.
Comment fonctionne s-SNOM
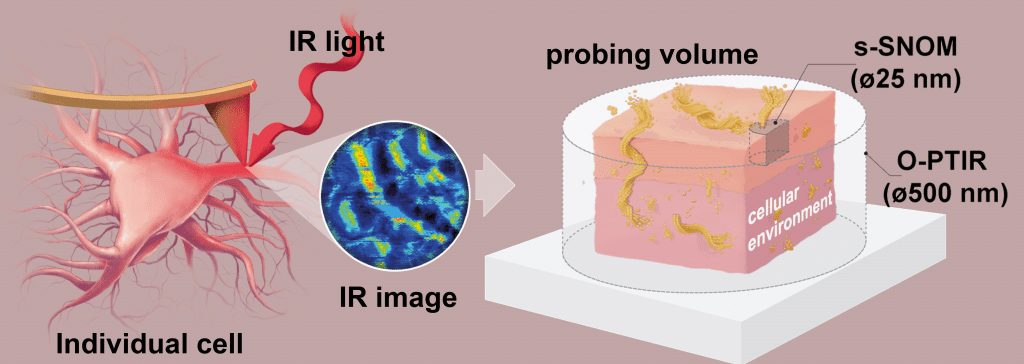
Le s-SNOM est une technique d'imagerie puissante qui combine la microscopie à force atomique (AFM) et l'imagerie spectrale infrarouge (IR). Elle permet aux scientifiques d'étudier les structures amyloïdes avec une résolution spatiale de 20 à 30 nm, bien supérieure à ce que les techniques de microscopie conventionnelles peuvent atteindre. Cette résolution remarquable permet aux chercheurs d'identifier et de cartographier les structures moléculaires, ce qui leur permet d'étudier plus en détail l'agrégation des protéines.
Le rôle de l'or ultra-plat
Dans cette étude, les chercheurs ont utilisé or ultraplat de Platypus Technologies afin de créer un environnement propice à l'imagerie haute résolution des neurones primaires. La surface recouverte d'or a constitué une plate-forme idéale pour la culture des neurones, ce qui a permis aux chercheurs d'étudier les structures de feuillets Aβ directement dans les neurones primaires individuels à l'aide de la nano-imagerie s-SNOM et des mesures Nano-FTIR.
Principales conclusions et implications pour l'avenir
Cette recherche novatrice démontre le potentiel de la s-SNOM en tant qu'outil précieux pour les neurobiologistes qui peuvent ainsi étudier les structures amyloïdes à l'échelle nanométrique dans les neurones sans avoir besoin de recourir à l'immunomarquage. L'utilisation de l'or ultraplat de Platypus Technologies a joué un rôle crucial dans l'obtention d'images à haute résolution et d'informations précieuses sur les mécanismes moléculaires de la maladie d'Alzheimer.
Alors que nous continuons à percer les mystères de la maladie d'Alzheimer, des technologies avancées comme le s-SNOM, associées à des matériaux de haute qualité comme l'or ultraplat, peuvent aider les scientifiques à mieux comprendre les mécanismes sous-jacents de la maladie. Ces connaissances pourraient ouvrir la voie à des traitements plus efficaces et, en fin de compte, améliorer la vie des millions de personnes touchées par la maladie d'Alzheimer.